開発の経緯について
本剤は、ヒト血漿を分画して精製した静脈内注射用の乾燥濃縮人プロテイン C 製剤である。本剤の有効成分であるプロテイン C(PC)は、内因性 PC と同様に、血管内皮細胞表面のトロンビン/トロンボモジュリン複合体によって活性化 PC(APC)に変換されることで抗凝固作用を発揮する。そのため、本剤は、先天性 PC 欠乏症患者の静脈血栓塞栓症及び電撃性紫斑病の治療、並びに血栓形成傾向の抑制に有用と考えられる。
先天性 PC 欠乏症は、PC の量的欠損又は機能欠損を特徴とする遺伝性疾患であり、PC の欠乏により凝固亢進状態となることで、ときに致死的な血栓症を生じる。特にホモ接合体又は複合ヘテロ接合体の患者で PC 活性が 1%未満に著減している場合は、多くの患者が生後数時間~数日の間に重篤な臨床症状を発現する。電撃性紫斑病は先天性 PC 欠乏症患者の急性血栓性事象で最もよくみられる症状の一つであり、治療しなければ急速に出血性水疱へと発展するほか、壊疽性壊死に至った場合は四肢の切断が必要になることもある。その後、海外では、本剤の製造販売承認を取得するため、臨床試験及びコンパッショネートユース下の成績に基づき、先天性 PC 欠乏症患者における本剤の有効性、安全性及び薬物動態(PK)が評価された。その評価結果を踏まえ、本剤は、重度先天性 PC 欠乏症の治療薬として、欧州では 2001 年 7 月、米国では 2007 年 3 月に製造販売承認を取得しており、2023 年 3 月時点で、世界 40 ヵ国以上で販売されている。
本邦では、医療現場への意見聴取の結果、先天性 PC 欠乏症患者に対する急性期治療及び血栓形成傾向の抑制(短期補充及び長期補充)が可能な薬剤の開発が望まれていることが判明したことから、本剤の国内開発として国内第Ⅰ/Ⅱ相試験(TAK-662-1501 試験)を 2021 年 9 月から開始した。なお、非日本人の先天性 PC 欠乏症患者における本剤の PK、有効性及び安全性については、先天性 PC 欠乏症患者を対象とした海外第Ⅱ/Ⅲ相試験(IMAG-098 試験)及び海外第Ⅱ/Ⅲ相試験(400101 試験)において検討されている。TAK-662-1501 試験の PK 試験パートで日本人患者のPK を評価した結果、PK の個体間差が大きい結果となり、本剤を投与する際は、各患者の PC 活性をモニタリングし、投与レジメンを個別に調整する必要があることが示された。一方で、PK 試験パートを完了した被験者に対して治療選択肢として本剤の投与機会を提供するための継続試験パートでは、日本人患者における良好な治療成績が得られた。
以上の結果から、海外と同様に本邦においても、本剤は先天性 PC 欠乏症に対する治療選択肢になり得ると考えられ、2024 年 3 月に「先天性プロテイン C 欠乏症に起因する次の疾患の治療及び血栓形成傾向の抑制 ○静脈血栓塞栓症 ○電撃性紫斑病」の効能又は効果にて承認された。
作用機序
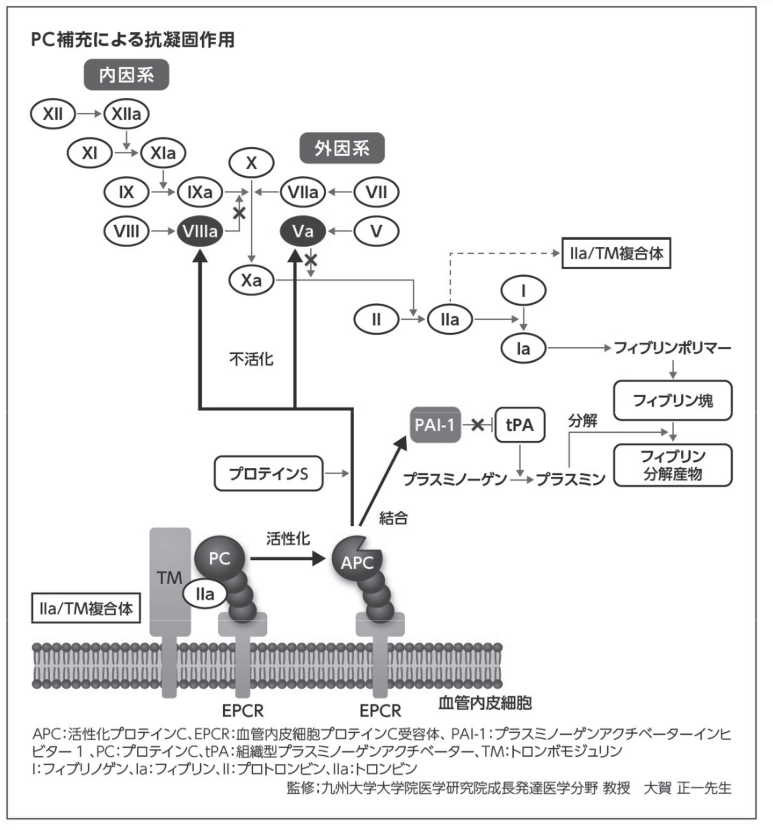
本剤の有効成分である PC はビタミン K 依存性の抗凝固因子であり、主に肝臓で合成され、血漿中では不活性なセリンプロテアーゼ前駆体として循環する。PC は血管内皮細胞膜上でトロンビン/トロンボモジュリン複合体により活性化され、抗凝固作用を有する APC に変換される。APCは補酵素であるプロテイン S の存在下で活性化第 V 因子(Va)及び活性化第 VIII 因子(VIIIa)を選択的に不活化し、凝固促進因子であるトロンビンの生成を抑制することにより抗凝固作用を示す。また、APC はプラスミノーゲンアクチベーターインヒビター1 に結合し、組織型プラスミノーゲンアクチベーターの活性を促進することにより、間接的な線溶促進作用を示す。さらに、Va 及び VIIIa の不活化によるトロンビン生成抑制により、トロンビン活性化線溶阻害因子の活性が抑制され、線溶促進作用をもたらす。
製品情報
| 商品名 | セプーロチン静注用1000単位 |
| 一般名 (洋名) | 乾燥濃縮人プロテイン C (Freeze-dried human protein C concentrate) |
| 承認年月日 | 2024年3月26日 |
| 発売年月日 | 2024年9月6日 |
| メーカー | 武田薬品工業株式会社 |
| 名前の由来 | Protein C のアルファベットの並び替えによる |
| ステム |
[こちらも参照:ステムで薬の名前を暗記!【一覧リスト】薬が覚えられない人必見!]
効能又は効果
先天性プロテインC欠乏症に起因する次の疾患の治療及び血栓形成傾向の抑制
- 静脈血栓塞栓症
- 電撃性紫斑病
注意
本剤は、ヒト血漿を原料として製剤化したものである。原料となった血漿を採取する際には、問診、感染症関連の検査を実施するとともに、製造工程における一定の不活化・除去処理等を実施し、感染症に対する安全対策を講じているが、ヒト血漿を原料としていることによる感染症伝播のリスクを完全に排除することはできないため、疾病の治療上の必要性を十分に検討の上、必要最小限の使用にとどめること。
用法及び用量
本剤を添付の注射用水全量で溶解し、緩徐に静脈内に投与する。
- 〈急性期治療及び血栓形成傾向の抑制における短期補充(周術期、抗凝固療法開始時等)〉通常、初回は100~120国際単位/kgを、次回以降3回は60~80国際単位/kgを6時間毎に投与し、その後は45~60国際単位/kgを6時間又は12時間毎に投与する。なお、患者の状態に応じて、投与量及び投与頻度を適宜増減する。
- 〈血栓形成傾向の抑制における長期補充〉通常、45~60国際単位/kgを12時間毎に投与するが、短期補充に用いる用法及び用量から開始することもできる。なお、患者の状態に応じて、投与量及び投与頻度を適宜増減する。
注意
・活性化プロテインC抵抗性の第Ⅴ因子変異を有する患者に対する本剤の効果は期待できない。
・本剤の投与量、投与頻度及び投与期間は、プロテインC活性を含む患者の状態に基づいて決定すること。
・本剤を投与する際は最大2mL/分の速度で緩徐に投与すること。ただし、体重10kg未満の小児には、0.2mL/kg/分を超えない速度でより緩徐に投与すること。
代謝・代謝酵素について
本剤に含まれる PC は内因性ヒトタンパク質であり、PC はトロンビンとトロンボモジュリンの複合体によって APC に変換された後、血漿中で PC インヒビター及び α1-アンチトリプシンによって代謝されて不活性化されることが知られている 。
食事の影響
該当データなし
副作用(抜粋)
重大な副作用として、重篤な過敏症、ヘパリン起因性血小板減少症、出血が認められた。
主な副作用は、そう痒、発疹、発熱、めまい(いずれも 5%未満)が認められた。
こちらのサイトは記載日時点の添付文書、インタビューフォームをまとめたものです。記載内容には十分な注意を払っておりますが、医療の情報は日々新しくなるため、誤り等がある場合がございます。参考にする場合は必ず最新の添付文書等をご確認ください。
情報更新日:2024年09月