エンホルツマブ ベドチン(以下、本剤)は、Nectin-4 を標的とする抗体薬物複合体(ADC)であり、アステラス製薬株式会社と Seagen Inc.が見出し、尿路上皮癌(UC)の治療薬として共同開発している。Nectin-4 は様々な癌、特に UC、乳癌、肺癌、膵癌、卵巣癌等に発現している接着タンパク質である。一部の癌では、Nectin-4 の高発現と病勢進行及び/又は予後不良との間の関連が報告されている 。Nectin-4 は UC 細胞表面に高発現していることから、理想的な治療標的となる。
本剤は、タンパク質分解酵素で切断されるバリン-シトルリン(vc)マレイミドカプロイルリンカーを介して、低分子の微小管阻害薬モノメチルアウリスタチン E (MMAE)を結合させた抗 Nectin-4 完全ヒト型免疫グロブリン G1κ モノクローナル抗体(mAb)である。本剤が細胞表面の標的分子 Nectin-4 に結合し、ADC-Nectin4 複合体を形成する。この複合体は、細胞内移行し、リソソームに輸送される。リソソームで vc リンカーがタンパク質分解酵素で切断されることにより、MMAE が放出される 。細胞内に放出された MMAE はチューブリン重合を阻害し、G2/M 期での細胞周期停止とアポトーシスを引き起こす。
本剤は、白金系抗悪性腫瘍剤及びプログラム細胞死受容体 1 (PD-1)又はプログラム細胞死リガンド 1 (PDL1)阻害剤による治療歴を有する局所進行性又は転移性 UC 患者を対象とした第Ⅱ相試験(国際共同第Ⅱ相試験[EV-201])のコホート 1 のデータを根拠として、2019 年に米国で迅速承認された。その後、白金系抗悪性腫瘍剤及び PD-1/PD-L1 阻害剤による治療歴を有する局所進行性又は転移性 UC 患者を対象とした国際共同第Ⅲ相試験[EV-301]、及び PD-1/PD-L1 阻害剤による治療歴を有し、シスプラチンに不適応である局所進行性又は転移性 UC 患者を対象とした国際共同第Ⅱ相試験[EV-201]コホート 2 の結果を根拠として、2021 年 7 月に FDA から正規承認を取得するとともに、シスプラチン不適応で治療歴のある局所進行性又は転移性 UC 患者への適応追加の承認を取得した。
本邦においては、Nectin-4 を発現している転移性 UC 又はその他の悪性固形腫瘍の患者を対象とした海外第Ⅰ相試験[EV-101]、日本人の局所進行性又は転移性 UC 患者を対象とした国内第Ⅰ相試験[EV-102]、EV-201 試験及び EV-301 試験を評価資料として承認申請を行った。本剤は厚生労働省より優先審査の指定を受け、「がん化学療法後に増悪した根治切除不能な尿路上皮癌」を効能又は効果として、2021 年 9 月に製造販売承認された。
作用機序
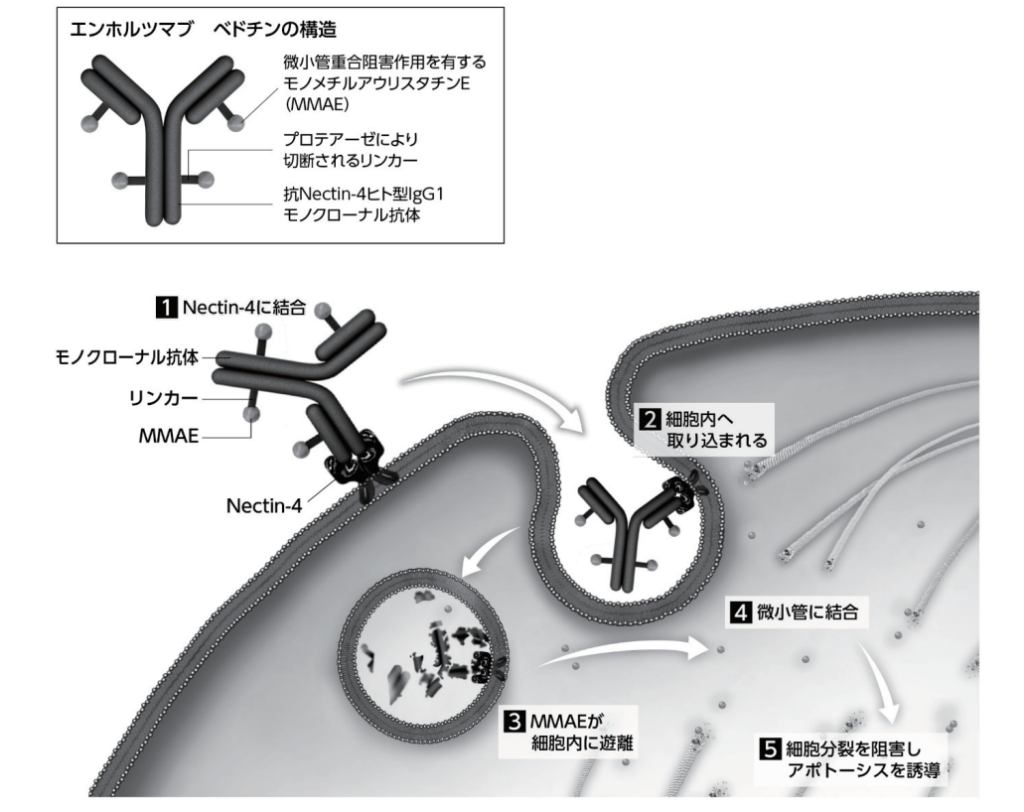
エンホルツマブ ベドチンは、尿路上皮癌細胞の表面に存在する接着蛋白である Nectin-4 を標的とする抗 Nectin-4 ヒト型 IgG1 モノクローナル抗体と、微小管重合阻害作用を有する MMAE を、リンカーを介して共有結合させた 抗体薬物複合体(ADC) である。エンホルツマブ ベドチンは、腫瘍細胞の細胞膜上に発現する Nectin4 に結合し、細胞内に取り込まれた後にプロテアーゼによりリンカーが切断され、MMAE が細胞内に遊離する。細胞内に遊離した MMAE は細胞内の微小管ネットワークを破壊し、続いて細胞周期を G2/M期に停止させ、アポトーシスを誘導すること等により、腫瘍増殖抑制作用を示すと考えられている。
製品情報
| 商品名 | パドセブ点滴静注用30㎎ |
| 一般名 (洋名) | エンホルツマブ ベドチン (Enfortumab Vedotin) |
| 発売年月日 | 2021年 11月 |
| メーカー | アステラス製薬株式会社 |
| 名前の由来 | PADCEV=Antibody-Drug Conjugate(抗体薬物複合体)+Enfortumab Vedotin(エンホルツマブ ベドチン) |
| ステム | ヒト型モノクローナル抗体:-umab |
[こちらも参照:ステムで薬の名前を暗記!【一覧リスト】薬が覚えられない人必見!]
効能又は効果
がん化学療法後に増悪した根治切除不能な尿路上皮癌
・本剤は、緊急時に十分対応できる医療施設において、がん化学療法に十分な知識・経験を持つ医師のもとで、本剤の使用が適切と判断される症例についてのみ投与すること。また、治療開始に先立ち、患者又はその家族に本剤の有効性及び危険性を十分説明し、同意を得てから投与すること。
・中毒性表皮壊死融解症(Toxic Epidermal Necrolysis:TEN)、皮膚粘膜眼症候群(Stevens-Johnson症候群)等の全身症状を伴う重度の皮膚障害があらわれることがあり、死亡に至った例も報告されている。以下の事項に注意するとともに、重度の皮膚障害が発現した場合には投与を中止し、適切な処置を行うこと。
・異常が認められた場合には、皮膚科医と連携の上、適切な処置(副腎皮質ホルモン剤、抗ヒスタミン剤の使用等)を行うこと。
本剤の成分に対し過敏症の既往歴のある患者
用法及び用量
通常、成人にはエンホルツマブ ベドチン(遺伝子組換え)として1回1.25mg/kg(体重)を30分以上かけて点滴静注し、週1回投与を3週連続し、4週目は休薬する。これを1サイクルとして投与を繰り返す。ただし、1回量として125mgを超えないこと。なお、患者の状態により適宜減量する。
PD-1/PD-L1阻害剤による治療歴のない患者における本剤の有効性及び安全性は確立していない。
代謝・代謝酵素について
本剤を構成するモノメチルアウリスタチンE(MMAE)はヒト肝ミクロソームにおいて主に CYP3A4 により代謝される。
食事の影響
該当データなし
副作用(抜粋)
重大な副作用として、重度の皮膚障害、高血糖(6.4%)、末梢性ニューロパチー(46.3%)、骨髄抑制、感染症(14.5%)、腎機能障害、間質性肺疾患(2.4%)が報告されている。
また、本剤が投与された 214 例中(日本人 14 例を含む)、203 例(94.9%)に副作用が認められた。いずれかのコホートでみられた主な副作用(20%以上)は、脱毛症 107 例(50.0%)、末梢性感覚ニューロパチー92 例(43.0%)、疲労 92 例(43.0%)、食欲減退 84 例(39.3%)、味覚不全 71 例(33.2%)、悪心 70 例(32.7%)、下痢61 例(28.5%)、そう痒症 59 例(27.6%)、斑状丘疹状皮疹 55 例(25.7%)、体重減少 52 例(24.3%)、貧血 49例(22.9%)及び皮膚乾燥 46 例(21.5%)であった。
情報更新日:2022年2月